
























Prepara tus exámenes y mejora tus resultados gracias a la gran cantidad de recursos disponibles en Docsity

Gana puntos ayudando a otros estudiantes o consíguelos activando un Plan Premium


Prepara tus exámenes
Prepara tus exámenes y mejora tus resultados gracias a la gran cantidad de recursos disponibles en Docsity
Prepara tus exámenes con los documentos que comparten otros estudiantes como tú en Docsity
Los mejores documentos en venta realizados por estudiantes que han terminado sus estudios
Estudia con lecciones y exámenes resueltos basados en los programas académicos de las mejores universidades
Responde a preguntas de exámenes reales y pon a prueba tu preparación

Consigue puntos base para descargar
Gana puntos ayudando a otros estudiantes o consíguelos activando un Plan Premium
Comunidad
Pide ayuda a la comunidad y resuelve tus dudas de estudio
Descubre las mejores universidades de tu país según los usuarios de Docsity
Ebooks gratuitos
Descarga nuestras guías gratuitas sobre técnicas de estudio, métodos para controlar la ansiedad y consejos para la tesis preparadas por los tutores de Docsity
Alquenos, Alquinos, Cetonas, Aldehídos y Ácidos Carboxílicos
Tipo: Apuntes
1 / 31

Esta página no es visible en la vista previa
¡No te pierdas las partes importantes!
























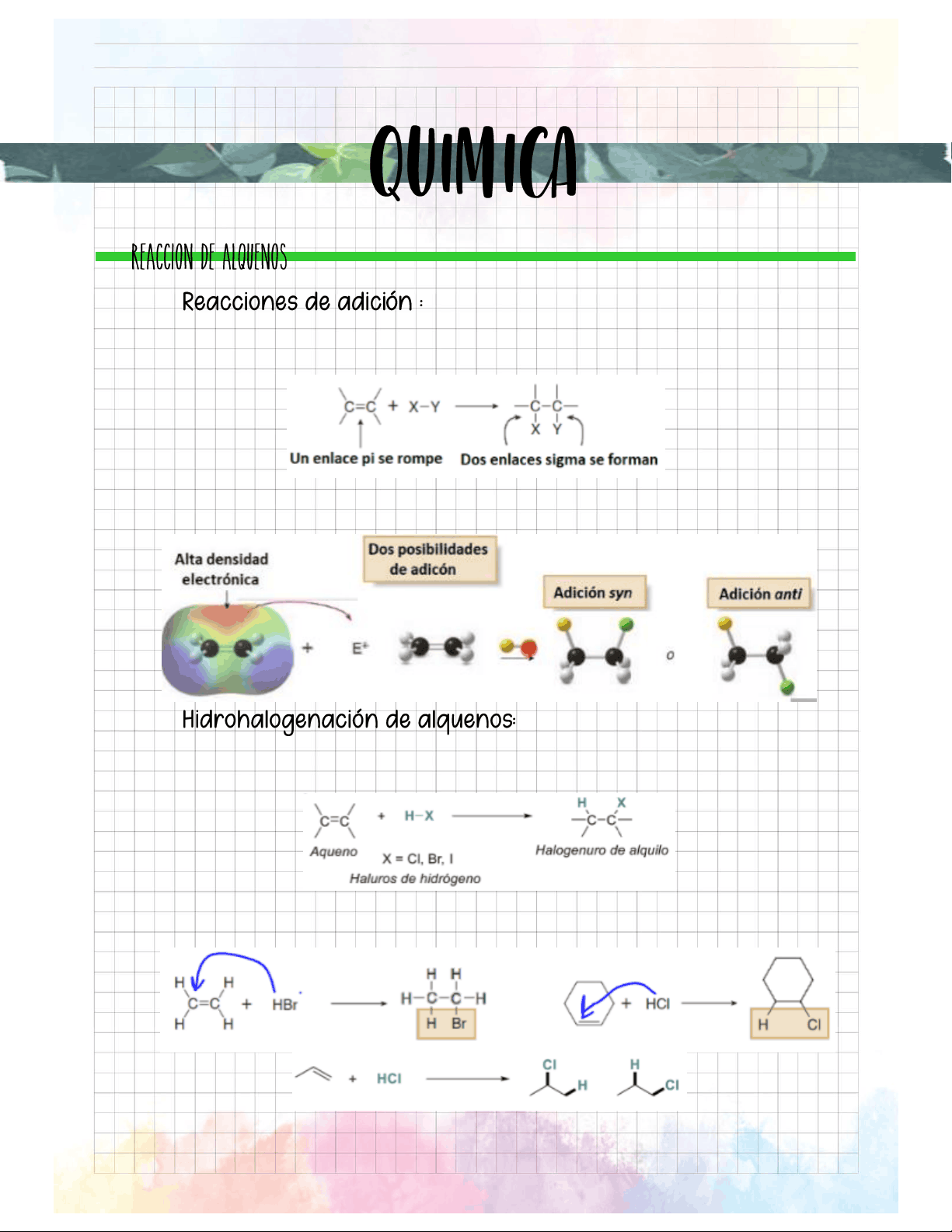
Debido a que el enlace PI de un C=C es más débil que el enlace sigma del C=C, este tiende a romperse, para formar dos enlaces sigma.
La función alqueno C=C es rica en densidad electrónica. Por eso, estas moléculas reaccionan con electrófilos, que son especies pobres en densidad electrónica.
Consiste en la adición haluros de hidrogeno (HCl, HBr, HI) a alquenos para formar halogenuros de alquilo.
.Dos enlaces se rompen en esta transformación: 1) El enlace pi débil del alqueno; 2) El enlace sigma del haluro. Para formar dos nuevos enlaces sigma.
Cuando se utilizan alquenos asimétricos, se obtiene un solo producto.
Durante la adición de un haluro de ácido (HX) a un alqueno asimétrico, el hidrógeno se adiciona al carbono menos sustituido, para formar así el carbocatión más estable. Ejercicios:
Consiste en la adición de agua o alcoholes a alquenos para formar alcoholes o éteres, respectivamente. La reacción se lleva a cabo en presencia de ácido como catalizador.
Los halogenuros de vinilo tienen un enlace pi que puede sufrir una segunda adición por parte de otro haluro de hidrógeno (HCl, HBr, HI) para formar un dihalogenuro de alquilo. La adición de HX sigue la regla de Markovnikov, y los dos halógenos resultan enlazados al mismo carbono.
Método para convertir un alquino C≡C en un alcano C-C o en un alqueno C=C empleando hidrógeno molecular como reactivo y catalizadores específicos.
Ejercicios:
Consiste en la adición de agua a alquinos para formar cetonas cuando la reacción se lleva a cabo en medio activo y en presencia de sulfato de mercurio (HgSO4).
Tautomería: Interconversión de dos estructuras por la posición de un doble enlace.
Tautómeros: Isómeros constitucionales que difieren en la locación de un doble enlace y un hidrógeno, y que coexisten en un equilibrio.
Siempre se utilizará una de las estructuras de resonancia, no la estructura hibrida, con el fin de poder analizar los pares de electrones de los enlaces pi.
La molécula de benceno es plana, con cada átomo de carbono con hibridación sp2, formando ángulos de enlace de 120° y un orbital p vacío que se ubica por encima y debajo del plano.
Los 6 orbitales p vacíos que se ubican por encima y debajo del plano, se solapan entre sí para deslocalizar los electrones de cada orbital. Así, se forma una especie de “rosquillas” donde se ubica toda la densidad electrónica del benceno.
Para nombrar anillos de benceno con un sustituyente, se nombra el sustituyente y se adiciona la palabra benceno.
Algunos bencenos monosustituidos tienen nombres comunes tales como:
Existen tres formas diferentes en las cuales dos grupos pueden estar enlazados a un anillo de benceno. Para cada una de ellas existe un prefijo: orto, meta, para.
Si los dos grupos enlazados al anillo de benceno son diferentes, los sustituyentes se nombran en orden alfabético como prefijo a la palabra benceno.
Si uno de los sustituyentes hace parte de un nombre común, la molécula se nombra como un derivado monosustituido de ese “benceno común”.
Primer Paso: Se numera el anillo de tal forma que los sustituyentes tengan la secuencia numérica más baja.
Consiste en la sustitución de un hidrógeno por un halógeno (Cl2 o Br2) en presencia de catalizadores específicos como ácidos de Lewis.
Consiste en la sustitución de un hidrógeno por un grupo nitro (-NO2) en presencia de ácido nítrico (HNO3) y ácido sulfúrico (H2SO4).
Consiste en la sustitución de un hidrógeno por un grupo sulfónico (-SO3H) en presencia de óxido de azufre (SO3) y ácido sulfúrico (H2SO4).
Consiste en la sustitución de un hidrógeno por un grupo alquilo (-R) en presencia de halogenuro de alquilo (RX) y cloruro de aluminio (AlCl3).
Consiste en la sustitución de un hidrógeno por un grupo acilo (-COR) en presencia de un cloruro de ácido (RCOCl) y cloruro de aluminio (AlCl3).
Cuando los efectos directores de dos grupos se refuerzan, el electrófilo se adiciona en la posición dirigida por los dos grupos.
Reacción para transformar un grupo metilo (-CH3) en un grupo carboxílico (-COOH).
Reacción para transformar un grupo nitro (-NO2) en un grupo amino primario (-NH2).
Es un proceso en el que se forma un nuevo enlace pi tras la eliminación de los grupos
Regla de Zaitsev Establece que en una reacción de eliminación B, en la que pueda ser formado más de un alqueno, se formará el alqueno más estable, es decir, el más sustituido.
Los alcoholes sufren reacciones de sustitución a través de la catálisis con haluros de hidrógeno (HCl, HBr, HI) o con reactivos halogenados (SOCl2, PBr3) para formar halogenuros de alquilo.
Ejemplos:
Los alcoholes se pueden oxidar para formar una variedad de compuestos carbonilicos
Alcoholes primarios: Se pueden oxidar en aldehídos o ácidos carboxílicos dependiendo de las condiciones de reacción.
Consiste en la sustitución halogenuros de alquilo (R-X) por un grupo alcóxido (-OR).
Consiste en la hidrólisis (ruptura) de los dos enlaces C-O el éter por parte de ácidos fuertes (HBr, HI) para formar dos halogenuros de alquilo (R-X y R’-X).
Cuando son éteres aromáticos-alifáticos, el fragmento aromático no se halógena, se hidroliza para formar un fenol, mientras que el fragmento alifático si forma el respectivo halogenuro de alquilo.
Los aldehídos son compuestos orgánicos caracterizados por poseer el grupo funcional - CHO. Se denominan como los alcoholes correspondientes, cambiando la terminación -ol por -al : Es decir, el grupo carbonilo H-C=O. está unido a un solo radical orgánico.
Los aldehídos se pueden oxidar en presencia de oxidantes fuertes para formar ácidos carboxílicos.
Los aldehídos se pueden reducir en presencia de agentes reductores, borohidruro de sodio (NaBH4), para formar alcoholes.